Interview met prof. Tombal: Moeten alle prostaatkankers worden behandeld?
 Professor Bertrand Tombal is het hoofd van de urologieafdeling van de ‘Cliniques Universitaires de Louvain’ (UCL, Woluwe). Hij bekleedde tevens de functie van voorzitter bij de ‘European Organisation for Research and Treatment of Cancer’ (EORTC), de toonaangevende Europese academische onderzoeksorganisatie op het gebied van kanker.
Professor Bertrand Tombal is het hoofd van de urologieafdeling van de ‘Cliniques Universitaires de Louvain’ (UCL, Woluwe). Hij bekleedde tevens de functie van voorzitter bij de ‘European Organisation for Research and Treatment of Cancer’ (EORTC), de toonaangevende Europese academische onderzoeksorganisatie op het gebied van kanker.
Zijn klinische expertise richt zich specifiek op urologische oncologie, met de nadruk op prostaat- en blaaskanker. Het voornaamste interessegebied van professor Bertrand Tombal betreft de behandeling van de gevorderde stadia van prostaatkanker, met speciale aandacht voor de hormonale therapie en voor de ontwikkeling van nieuwe biologische middelen. Hij coördineert meerdere, grootschalige klinische studies op dit gebied. Professor Tombal heeft bovendien meer dan 300 wetenschappelijke artikels, boeken en boekhoofdstukken geschreven en hij is een graag geziene presentator op vele nationale en internationale wetenschappelijke congressen. De redactie van ‘De medische referentie’ heeft met genoegen vastgesteld dat professor Bertrand Tombal bereid was om uitvoerig antwoord te geven op een reeks uiteenlopende vragen over prostaatkanker.
Prostaatkanker is in België de vaakst gediagnosticeerde kanker bij mannen van 50 jaar en ouder. Welke verschillende soorten prostaatkanker zijn er?
Professor Bertrand Tombal: Prostaatkanker is een zeer heterogene aandoening. De eerste stap bij de diagnose van prostaatkanker bij een individuele patiënt bestaat uit de classificatie van de prostaatkanker op basis van de gradering (hoe agressief is de prostaatkanker?) en op basis van het stadium (waar bevindt de prostaatkanker zich?).
De Gleason-score is een classificatiesysteem dat wordt gebruikt om de agressiviteit van prostaatkanker te beoordelen. Het is vernoemd naar Dr. Donald Gleason, een patholoog die het systeem in de jaren 1960 heeft ontwikkeld. De Gleason-score wordt meestal bepaald door een patholoog op basis van het onderzoek van prostaatweefsel dat is verkregen uit een biopsie. De Gleason-score is gebaseerd op de microscopische kenmerken van de prostaatkankercellen. Het omvat twee componenten: het primaire patroon en het secundaire patroon. Het primaire patroon is het meest voorkomende patroon van kankercellen in het weefselmonster, terwijl het secundaire patroon het op één na meest voorkomende patroon is. Elk patroon krijgt een score op een schaal van 1 tot 5, waarbij 1 overeenkomt met goed gedifferentieerde cellen die lijken op normaal prostaatweefsel en 5 overeenkomt met slecht gedifferentieerde cellen die erg afwijken van normaal weefsel. De Gleason-score wordt verkregen door de scores van het primaire en secundaire patroon op te tellen. De Gleason-score is een belangrijke factor bij het bepalen van de behandelingsopties en het voorspellen van de prognose voor mannen met prostaatkanker. Tegenwoordig wordt deze score gebruikt zoals aangepast door de ISUP (International society of Uropathology): de ISUP-graden variëren van 1 tot 5.
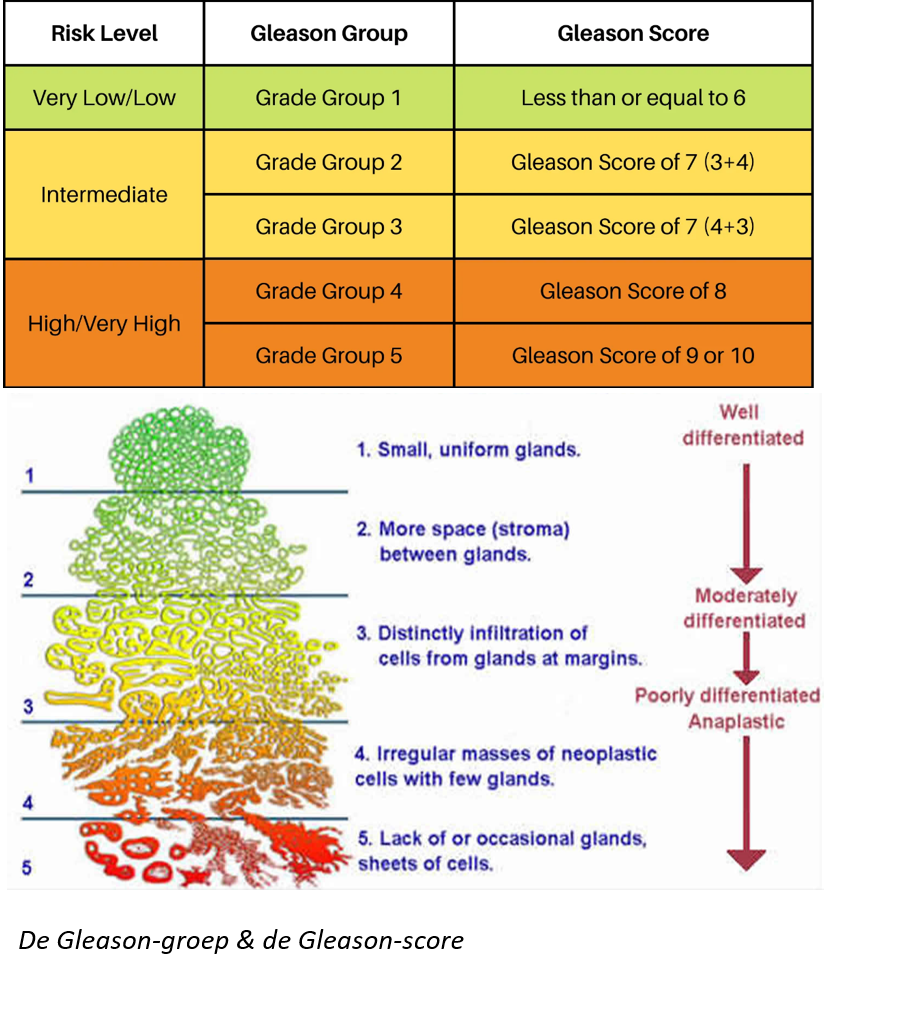
Bron: https://www.prostateconditions.org/about-prostate-conditions/prostate-cancer/newly-diagnosed/gleason-score
Het prostaat specifiek antigeen (PSA) is een eiwit dat wordt geproduceerd door de prostaat. PSA kan in kleine hoeveelheden in het bloed worden gevonden en de meting van PSA-niveaus wordt gebruikt als een marker voor prostaatgezondheid en de detectie van prostaatproblemen, zoals prostaatkanker. Het PSA-niveau kan ook stijgen bij benigne prostaathypertrofie. Het gebruik van PSA-tests voor prostaatkankerscreening is controversieel. Hoewel het bepalen van het PSA-niveau kan helpen bij het opsporen van prostaatkanker, kan het ook leiden tot een overdiagnose en overbehandeling van tumoren die zeer langzaam groeien of niet levensbedreigend zijn. Concreet wordt aangeraden om bij een patiënt met een beperkt verhoogde PSA-waarde (< 10 mg/L) bij wie een MRI aantoonde dat de tumor gelokaliseerd is in de prostaat en bij wie de Gleason-graad (ISUP) 1 of 2 bedraagt, geen behandeling op te starten en deze patiënt actief op te volgen. Het concept van actieve opvolging startte ongeveer 20 jaar geleden – maar in België is het nog niet volledig geïmplementeerd en we zien dat er nog veel patiënten in ons land een agressieve behandeling krijgen wanneer dit niet nodig is. Nochtans pleit het Federaal Kenniscentrum (KCE) al meer dan een decennium om bij een lokale prostaatkanker te overwegen om eerst aan actieve opvolging te doen. De prostaattumor wordt dan regelmatig opgevolgd en zodra er progressie wordt vastgesteld, wordt er een klassieke behandeling opgestart. Een klassieke behandeling van prostaatkanker zorgt regelmatig voor ernstige nevenwerkingen die de levenskwaliteit aantasten (door o.a. incontinentie en/of impotentie). Bij een actieve opvolging worden er regelmatig een MRI, een PSA-test en nieuwe biopsieën uitgevoerd. De keuze voor actieve opvolging is voor vele patiënten en ook artsen niet gemakkelijk. De eenvoudigste oplossing is de intuïtie te volgen en de kanker te verwijderen, zelfs als de patiënt daarmee niet altijd het best geholpen is. Bij de diagnose van prostaatkanker moet het belangrijkste gespreksonderwerp met de patiënt niet zijn welke behandeling er moet worden opgestart, maar wel wat de kenmerken van de individuele prostaatkanker zijn. Als het een indolente kanker betreft, is de beste oplossing geen actieve behandeling, maar een actieve opvolging.
Kan u dieper ingaan waarom een opvolging volstaat bij het merendeel van de prostaatkankers?
Professor Bertrand Tombal: Bij ongeveer 50% van alle patiënten die de diagnose prostaatkanker krijgen, is een actieve opvolging de beste optie. Een actieve opvolging kan bijvoorbeeld uit een jaarlijkse MRI-opname en een regelmatige controlebiopsie na 2 of 3 jaar bestaan. Al 15 jaar geleden werd aangetoond dat het risico op overlijden aan de gevolgen van een indolente prostaatkanker zeer laag is. Grootschalige klinische studies – waaronder de PROTECT-studie – hebben dit aangetoond. Tussen 1999 en 2009 werden in de PROTECT-studie 2.664 mannen in het Verenigd Koninkrijk met gelokaliseerde prostaatkanker gerandomiseerd naar chirurgie of onmiddellijke radiotherapie of actieve monitoring. Na 15 jaar opvolging trad overlijden aan prostaatkanker op bij 3,1% van de mannen in de actieve opvolgingsgroep, 2,2% in de prostatectomiegroep en 2,9% in de radiotherapiegroep. (P = 0,53 voor de algemene vergelijking). Hormonale therapie werd gestart bij 12,7% van de patiënten in de actieve monitoringgroep, 7,2% in de chirurgiegroep en 7,7% in de radiotherapiegroep.
Dit suggereert dat actieve opvolging een veilige optie was voor mannen met gelokaliseerde prostaatkanker. Actieve opvolging is niet uniek voor prostaatkanker, maar wordt ook gezien bij bijvoorbeeld huidkankers zoals basocellulaire carcinoma of bij sommige vormen van chronische leukemie.

Overleving van prostaatkanker in de PROTECT-studie in de patiëntengroep die actief opgevolgd werd, in de prostatectomiegroep en in de radiotherapiegroep.
Bron: Hamdy FC, et al. Fifteen-year outcomes after monitoring surgery, or radiotherapy for prostate cancer. The New England Journal of Medicine 2023; 388: 1547-1558.
Leidt een verhoogde PSA-waarde of een afwijkend rectaal toucher automatisch tot het uitvoeren van een prostaatbiopsie?
Professor Bertrand Tombal: Dit zou niet mogen. Deze aanpak leidt immers tot een overbehandeling. Vandaag zou een verhoogde PSA-waarde de artsen moeten motiveren tot het uitvoeren van een transrectale echografie. De meest voorkomende reden van een verhoogde PSA-waarde is een benigne prostaathyperplasie. Als de transrectale echografie enkel een vergrote prostaat aantoont, kan de patiënt gerustgesteld worden. Indien de transrectale echografie afwijkend is, moet de patiënt een MRI ondergaan. De toegang tot kwaliteitsvolle multiparametrische MRI-opnamen is in België uitstekend. Wanneer er een verdacht letsel zichtbaar is op de MRI-beeldvorming kan een doelgerichte biopsie worden afgenomen. Deze aanpak vermindert het risico op het opsporen van indolente kankers en het helpt om agressieve kankers niet te missen.
Bij de detectie van een agressieve prostaatkanker met een vermoeden van metastase is een verdere evaluatie aan de hand van een PSMA PET-scan mogelijk om aldus de prostaatkanker volledig in beeld te brengen. PSMA staat voor ‘Prostaat Specifiek Membraan Antigeen’, een eiwit dat zich in hoge concentraties bevindt op het oppervlak van de prostaatkankercellen. Tijdens een PSMA PET-scan krijgt de patiënt een injectie met een radioactief gelabelde molecule die zich bindt aan het PSMA-eiwit. Deze radioactieve molecule wordt meestal gecombineerd met een stof die de straling uitzendt, zodat het kan worden gedetecteerd door een PET-scanner. Deze beelden kunnen artsen helpen bij het beoordelen van de omvang van de ziekte, het opsporen van de uitzaaiingen naar andere delen van het lichaam en het begeleiden van de behandeling.
In de toekomst zal de introductie van ‘high frequency’ transrectale echografie – waarmee meer gedetailleerde beelden van de prostaat kunnen gevisualiseerd worden – wellicht de MRI-opnamen kunnen vervangen. In België wordt ‘high frequency’ transrectale echografie nog maar amper gebruikt.
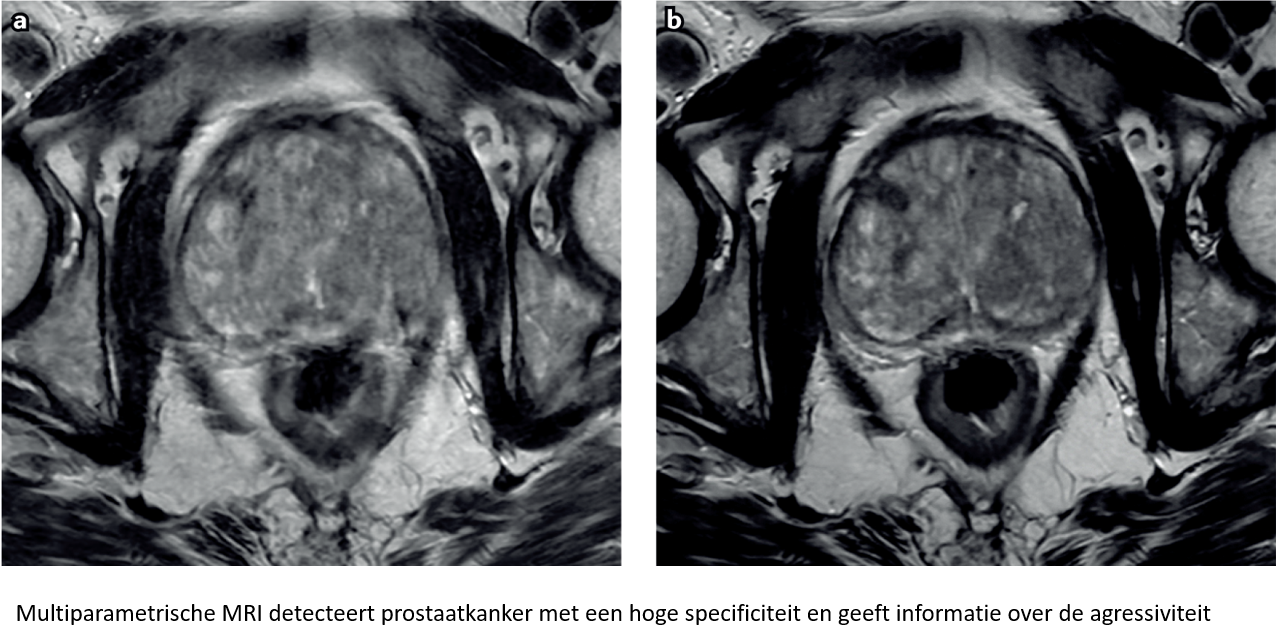
Bron: patient files Tombal, met toestemming gebruikt
Wat is de standaardbehandeling voor patiënten met prostaatkanker?
Professor Bertrand Tombal: De standaardbehandeling van prostaatkanker is verrassend genoeg geen behandeling. Bij de helft van de patiënten met prostaatkanker volstaat het actief opvolgen en moet er geen actieve behandeling opgestart worden. De eerste boodschap die een arts moet meedelen aan een patiënt die gediagnosticeerd wordt met prostaatkanker is of zijn prostaatkanker al dan niet een behandeling vereist. Zo stellen de richtlijnen van het Federaal Kenniscentrum voor de Gezondheidszorg dat bij patiënten met een levensverwachting van minder dan 10 jaar of bij patiënten die ook lijden aan andere ernstige aandoeningen (diabetes, hartfalen, andere kanker, enz.) moet overwogen worden om helemaal niet te behandelen. Een zware behandeling, die gepaard gaat met pijnlijke bijwerkingen kan de levenskwaliteit van deze patiënten in de laatste jaren van hun leven immers in sterke mate ondermijnen. De voor- en nadelen van een prostaatkankerbehandeling – die per patiënt verschillen en die afhangen van de globale gezondheid en de levensverwachting en van de risicocategorie van de kanker – moeten dus goed tegen elkaar worden afgewogen. Het volgen van de laatste nieuwe behandeling is dus niet altijd de beste keuze. Dankzij de zogenaamde “actieve monitoring” (niet tussenkomen maar regelmatig onderzoeken om de evolutie van de tumor op te volgen) kan er soms 10 jaar worden gewacht voordat een behandeling moet worden opgestart, zonder dat de levensverwachting daarbij wordt ingekort. Alleen wanneer er aanwijzingen zijn dat de kanker progressie vertoont, wordt onmiddellijk een behandeling opgestart.
Sommige patiënten wensen echter gemoedsrust en zullen aandringen op de heelkundige verwijdering van de prostaatkanker. Een prostatectomie is echter geassocieerd met een belangrijk risico op erectiele dysfunctie en risiso op incontinentie. Patiënten voor wie hun seksueel leven heel belangrijk is en die om deze reden geen prostatectomie zullen aanvaarden zullen sneller voor radiotherapie kiezen. De radiotherapie kende een snelle en grondige evolutie en in verschillende centra in België zal de patiënt met prostaatkanker slechts vijf cycli moeten ondergaan. Voor deze lokale behandeling moet er ook geen systematische bijkomende hormoontherapie opgestart worden. Het belangrijkste is dat patiënten gerustgesteld worden dat geen enkele prospectieve gerandomiseerde studie een verschil heeft aangetoond in termen van vermindering van het risico op uitzaaiingen of overlijden. Chirurgen stellen vaak dat als er een recidief is na radiotherapie, een operatie niet langer een optie is. Geïsoleerde lokale recidieven zijn zeldzaam (< 5% voor intermediair-risicokankers). In alle gevallen moet de patiënt met een prostaatkankerdiagnose voldoende informatie ontvangen zodat hij zelf de behandelingskeuze kan maken. In de ideale wereld zou de patiënt dan ook zowel een radiotherapeut als een uroloog moeten kunnen spreken om vervolgens de behandelingskeuze te maken, en mogelijk ook een ervaren verpleegkundige, die a priori minder vooringenomen is in zijn of haar uitleg.

Algoritme voor de behandeling van gelokaliseerde prostaatkanker
Bron: KCE Report 226AS.
De behandeling van gemetastaseerde, hormoon-gevoelige prostaatkanker kende het voorbije decennium een grondige evolutie dankzij diverse combinatiebehandelingen. Kan u uw visie hierop delen?
Professor Bertrand Tombal: Patiënten moeten zich bewust zijn van het feit dat een therapie met een combinatie van androgeendeprivatie en een hormoon van de derde generatie de standaardbenadering is bij de behandeling van gemetastaseerde prostaatkanker. Voor gemetastaseerde, hormoongevoelige prostaatkanker zijn er vier geneesmiddelen beschikbaar: abirateronacetaat (Zytiga®), apalutamide (Erleada®), enzalutamide (Xtandi®) en darolutamide (Nubeqa®). Omdat er geen significante, maar enkel subtiele, verschillen zijn in de doeltreffendheid en de bijwerkingen tussen deze geneesmiddelen, is het belangrijk om de geschikte behandeling te kiezen op basis van de individuele patiënt. Deze geneesmiddelen worden standaard gebruikt bij hormoongevoelige prostaatkanker met uitzaaiingen en ze zullen worden aangevuld met een lokale therapie of een chemotherapie. Een discussie die de laatste tijd steeds meer aandacht krijgt, is deze over de duur van de behandeling en hoe dit van invloed is op de levenskwaliteit van de patiënt. Het is belangrijk om deze aspecten in overweging te nemen en individueel met de patiënt te bespreken.
Welke nieuwe geneesmiddelen zijn er vandaag beschikbaar voor de behandeling van mannen met uitgezaaide prostaatkanker en in welke specifieke omstandigheden worden deze gebruikt?
Professor Bertrand Tombal: Ik zou twee nieuwe geneesmiddelenklassen willen vermelden die hun plaats hebben bij de patiënten met gemetastaseerde prostaatkanker die na een eerstelijnsbehandeling ziekteprogressie vertonen.
Ten eerste zijn er de PARP-inhibitoren (poly ADP ribose polymerase): olaparib (Lynparza®) en andere stoffen waarvan de registratieprocedure loopt. Dit zijn geneesmiddelen die van groot belang zijn voor de patiënten met specifieke genmutaties, zoals BRCA1- en BRCA2-mutaties. Deze geneesmiddelen worden vooral gebruikt wanneer er ziekteprogressie optreedt. Helaas is er in België nog te weinig aandacht voor het testen op deze mutaties. Het is van essentieel belang dat artsen vroeg in de ziekte zoeken naar deze mutaties, omdat ze bij 5 tot 10% van de patiënten aanwezig zijn. Als een patiënt de BRCA1- en/of BRCA2-mutaties heeft, worden de PARP-inhibitoren bij ziekteprogressie na de initiële behandelingen beschouwd als de standaardbehandeling. De tweede nieuwe behandeling is de radionuclide therapie voor prostaatkanker. Dit is een vorm van gerichte, interne radiotherapie die gebruikt wordt bij de behandeling van gemetastaseerde prostaatkanker. Bij deze therapie wordt een radioactieve stof – lutetium-177 gekoppeld aan een ligand voor prostaatspecifiek membraanantigeen – intraveneus toegediend. Deze stof kan specifiek de prostaatkankercellen bereiken en er een gerichte straling afgeven. Deze therapie bestaat uit 4 tot maximaal 6 intraveneuze giften van Lu-177-PSMA, gegeven met tussenpozen van 4 weken. De bijwerkingen zijn gering en betreffen vooral xerostomie, vermoeidheid en geringe beenmergdepressie. In België beschikken we vandaag over vijf centra waarin deze behandeling gegeven wordt.
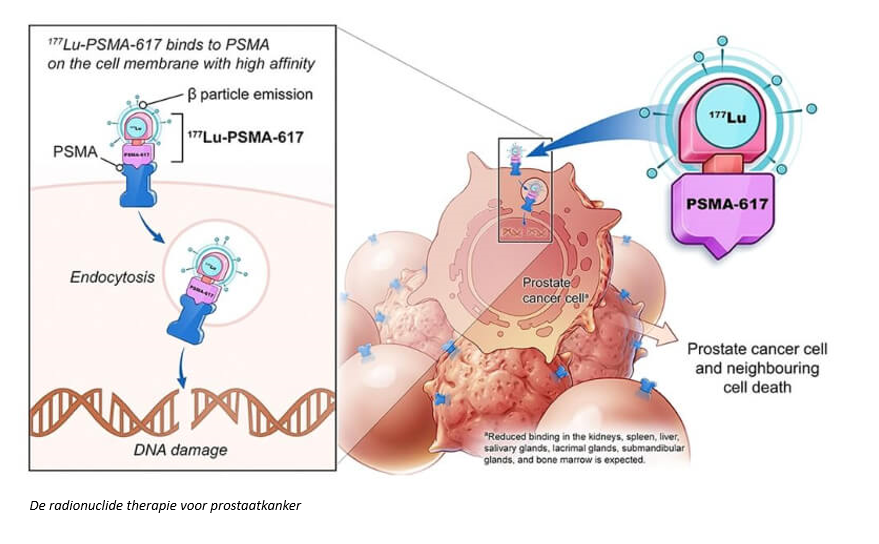
Bron: https://bookingmedtravel.com/blog/Lu-177-PSMA-therapy
Wat is uw ervaring bij het informeren van de patiënt met prostaatkanker over de mogelijke bijwerkingen van de behandelingen?
Professor Bertrand Tombal: Het aanbieden van voldoende en correcte informatie aan de patiënt is zeer belangrijk. Bij het informeren van patiënten met prostaatkanker over de mogelijke bijwerkingen van de behandelingen is mijn ervaring dat een holistische aanpak essentieel is. Het monitoren van bijwerkingen, het aanbieden van lichaamsbeweging en van psychologische ondersteuning, het beschikbaar maken van dieetbegeleiding en het geven van gedetailleerde uitleg aan de patiënt dragen allemaal bij aan het verbeteren van de zorgervaring en aan het welzijn van de patiënt. Door open communicatie en uitgebreide informatie streven we ernaar de patiënt volledig bewust te maken van wat hij kan verwachten tijdens zijn behandelingstraject en hoe hij met eventuele bijwerkingen kan omgaan.
Interview: Dr. Ph. Malaise
Het interview is met toestemming overgenomen uit De medische referentie – La référence médicale – nummer 6 (juni/ juli 2023).
Deze pagina is mogelijk gemaakt door:
