In deze rubriek belicht dr. Jorn Bovenschen, dermatoloog Máxima Medisch Centrum in Veldhoven en Eindhoven, nieuwe middelen of methoden. Wat gaan ze betekenen in het therapeutische landschap?
Inleiding
Het lifetime-risico op het krijgen van non-melanoma skin cancer (NMSC) is inmiddels opgelopen tot 1 op de 5 personen.1 De incidentie is nog steeds groeiende. In de praktijk zijn er bovendien veel meer individuele patiënten met veel grotere hoeveelheden huidmaligniteiten dan jaren geleden. Met name voor groepen hoogrisicopatiënten (orgaantransplantatiepatiënten, patiënten met een verzwakt immuunsysteem, patiënten met extreme zonblootstelling in het verleden) is de dermatologische zorg daarom vaak lastig, tijdrovend en suboptimaal. Het zou wenselijk zijn om middelen voorhanden te hebben om de stortvloed aan huidmaligniteiten in deze patiëntengroepen te kunnen reduceren.
Chemopreventie
Uiteraard is het routinematig en consistent aanbrengen van zonnebrandmiddelen de meest voorkomende vorm van topicale profylaxe tegen het ontwikkelen van NMSC. Omdat de therapietrouw van zonnebrandmiddelengebruik ook voor hoogrisicopatiënten over het algemeen vrij laag wordt ingeschat, zijn aanvullende preventieve maatregelen vooral in deze groep patiënten meer en meer noodzaak aan het worden.2
De laatste jaren is daarom er steeds meer aandacht voor systemische chemopreventie. We onderscheiden hierbij het aloude middel acitretine en het ‘upcoming’ nicotinamide.
Acitretine
De meeste ervaring met acitretine is opgedaan bij patiënten met een orgaantransplantatie in het verleden, die op langdurige medicamenteuze immuunsuppressie staan ingesteld. Het exacte werkingsmechanisme van acitretine in het kader van NMSC-reductie is niet geheel bekend, maar hypothesen omvatten: het normaliseren van cellulaire differentiatie, immuunmodulatie, inhibitie van tumordifferentiatie en -promotie door inductie van groeiarrest en apoptose van tumorcellen.3
Bavinck et al. lieten zien dat bij 38 nierrecipiënten die 6 maanden acitretine 30 mg 1dd gebruikten, het aantal actinische keratosen (AKs) 13,4% daalde. In de placebogroep was een stijging te zien van 28,2%; daarom een significant verschil van 41,6%. Daarnaast ontwikkelden patiënten in de acitretinegroep in deze 6 maanden 2 nieuwe plaveiselcelcarcinomen (PCCs) en in de placebogroep waren dit er 18.4
In een studie van George et al. kregen 23 nierrecipiënten in een prospectieve crossover-trial gedurende 2 jaar 25 mg acitretine. Het aantal nieuw ontwikkelde PCCs was statistisch significant lager dan in de periode zonder acitretine. Een dergelijke trend werd ook gezien voor basaalcelcarcinomen (BCCs), maar deze was niet statistisch significant. Bijwerkingen waren een beperkende factor.5
In een retrospectieve studie werd eveneens een reductie van nieuwe PCCs gevonden gedurende actieve behandeling in de eerste drie jaar na het starten van acitretine, ten opzichte van het jaar voor het behandelen met dit medicament.3 Een recente systematische review liet ook een 60%- reductie zien van nieuwe PCCs in orgaantransplantatiepatiënten.6
Samenvattend laten kleine studies van suboptimale kwaliteit met acitretine als chemopreventief middel bij orgaantransplantatiepatiënten een consistente reductie zien van het optreden van nieuwe NMSC, in het bijzonder van PCCs.
Nicotinamide
Er is een toenemend aantal artikelen over het gebruik van nicotinamide (syn. niacinamide; de amidevorm van vitamine B3) als chemopreventief middel tegen het ontstaan van NMSC. Het hypothetische mechanisme hierachter is dat nicotinamide, de voorloper van nicotinamideadeninedinucleotide (NAD), UV-geïnduceerde ATP-depletie voorkómt waardoor DNA-herstel makkelijker kan worden bewerkstelligd. Het remt ook UV-geïnduceerde immuunsuppressie als DNA beschadigd is.7,8
In een placebogecontroleerde gerandomiseerde fase 3-studie, gepubliceerd in het NEJM ontvingen 386 hoogrisicopatiënten 2dd 500 mg nicotinamide of placebo gedurende 1 jaar. Na 1 jaar hadden patiënten in de nicotinamidegroep, statistisch significant, 23% minder NMSC. Er ontstonden zelfs 30% minder PCCs dan in de placebogroep. De reductie in AKs was op zijn hoogst 20%. Het aantal BCCs was 20% verlaagd in de nicotinamidegroep, maar dit laatste was niet statistisch significant. Een half jaar na het staken van nicotinamide was er geen verschil meer in aantal NMSC tussen de nicotinamide- en placebogroepen. In deze studie werden nierrecipiënten geëxcludeerd.2 In figuur 1 worden de resultaten schematisch weergegeven.
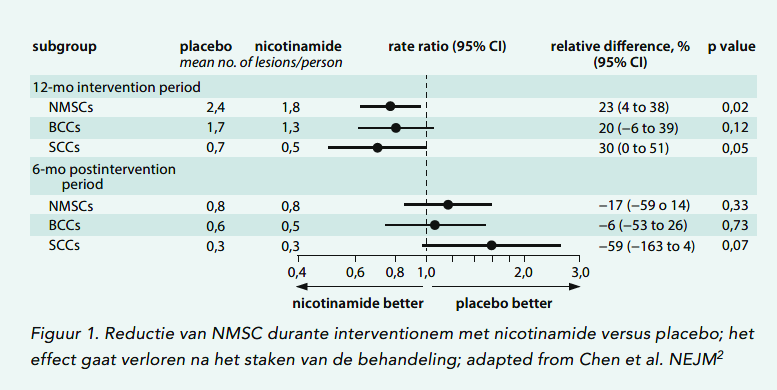
Figuur 1. Reductie van NMSC durante interventionem met nicotinamide versus placebo; het effect gaat verloren na het staken van de behandeling; Adapted from Chen et al. NEJM2
Toch zijn er voor nicotinamide ook enkele studies verricht bij orgaantransplantatiepatiënten, een populatie die sterk ‘at risk’ is vanwege de chronische immuunsuppressie. Drago et al. randomiseerden 24 nierrecipiënten (placebo of nicotinamide 3dd 250 mg gedurende 6 maanden) en rapporteerden reducties voor het optreden van AKs.9
Dezelfde auteur deed tevens een case-control-studie waarin 38 transplantatiepatiënten (8 lever- en 30 niertransplantatiepatiënten) met AKs, werden behandeld met nicotinamide 1dd 500 mg (19 cases); de andere patiënten kregen geen nicotinamide (19 controls). Na 6 maanden waren de AKs in de nicotinamidegroep bij 88% van de patiënten kleiner geworden. 42% van deze patiënten had bovendien complete regressie van de AKs en ontwikkelde geen nieuwe AKs. In de controlegroep liet 91% van de patiënten groei zien van bestaande AKs en ontwikkelden zij nieuwe AKs. In die 6 maanden werden 7 AKs in de controlegroep PCCs.10
Een placebogecontroleerde gerandomiseerde fase 2-studie met 22 niertransplantatiepatiënten liet zien dat nicotinamide veilig lijkt in deze populatie. Na 6 maanden behandeling was er een niet-statistisch significante trend richting verminderde aantallen NMSC in de nicotinamidegroep zichtbaar. Gemiddeld werden 4,2 nieuwe NMSC (BCCs en PCCs) gevonden in de placebogroep (95% BI 2,2–7,8; 45 NMSC in totaal) vergeleken met gemiddeld 2,7 nieuw ontwikkelde NMSC in de nicotinamidegroep (95% BI 1,4—5,3; 30 NMSC in totaal). Er was een niet-significante afname van 16% voor AKs in de nicotinamidegroep versus de placebogroep na 6 maanden (p = 0,15).11
Samenvattend worden ook voor nicotinamide relatief vergelijkbare gunstige resultaten gezien, met dien verstande dat deze wel onder meer in een placebogecontroleerde gerandomiseerde studie zijn aangetoond.2
Vergelijkende studie acitretine en nicotinamide
In een systematische review en meta-analyse van Tee et al. werd getracht de data van de verschillende studies betreffende acitretine en nicotinamide in de strijd tegen NMSC-ontwikkeling te vergelijken. Hoewel nicotinamide iets beter lijkt te werken dan acitretine in deze studie werd er geen statistisch significant verschil gevonden.12 In figuur 2 ziet u deze resultaten visueel weergegeven in een zogenaamde ‘network graph’.
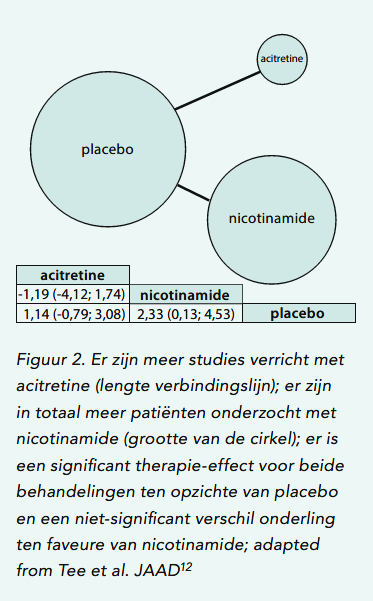
Figuur 2. Er zijn meer studies verricht met acitretine (lengte verbindingslijn); er zijn in totaal meer patiënten onderzocht met nicotinamide (grootte van de cirkel); er is een significant therapie-effect voor beide behandelingen ten opzichte van placebo en een niet-significant verschil onderling ten faveure van nicotinamide; adapted from Tee et al. JAAD12
Beschouwing
Zonprotectie en het adequaat gebruiken van zonnebrandmiddelen met een hoge beschermingsfactor blijft uiteraard de hoeksteen voor de preventie van NMSC. Echter, gezien de toename van patiënten met hoog risico op NMSC die chronisch multipele huidmaligniteiten ontwikkelen, wordt het inzetten van chemopreventief actieve middelen als acitretine en nicotinamide wenselijker, tot op heden wordt deze mogelijkheid te weinig benut.
Zowel acitretine als nicotinamide laten aantoonbaar gunstige resultaten zien om de toename van NMSC bij hoogrisicopatiënten te reduceren.2-6, 9-11 Het is nog geen duidelijk uitgemaakte zaak welk middel het beste werkt, vanwege het ontbreken van direct vergelijkend onderzoek van toereikend niveau.
Twee auteurs pleiten sterk voor het gebruik van nicotinamide ten opzichte van acitretine.8,13 Redenen die hiervoor worden aangedragen zijn samengevat in tabel 1. Samen met de resultaten van de vergelijkende meta-analyse12 lijkt er een voorkeur te zijn voor het gebruik van nicotinamide als middel van eerste keuze om de vloedgolf aan huidmaligniteiten bij hoogrisicopatiënten te kunnen beteugelen. Gezien de zeker aanwezige, maar niet daverend spectaculaire effectiviteit van beide middelen, zou het zeer interessant zijn om in direct vergelijkend prospectief gerandomiseerd dubbelblind onderzoek ook een arm met de combinatie van acitretine en nicotinamide mee te nemen om potentiële synergie en eventuele betere uitkomsten te kunnen evalueren.
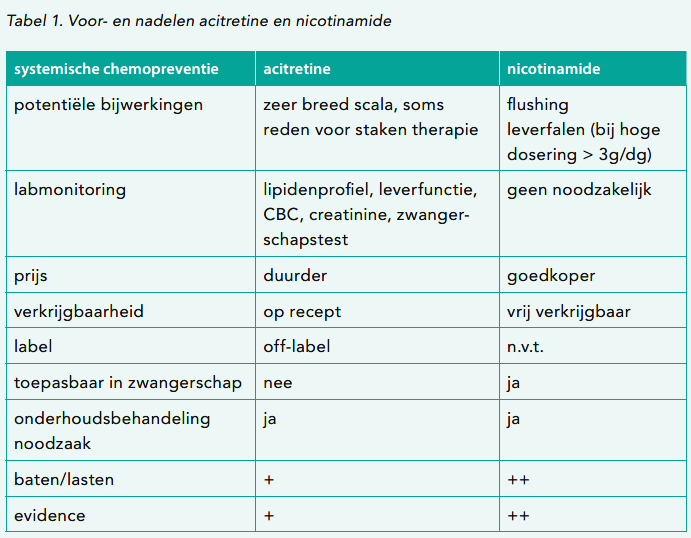
Tabel 1. Voor- en nadelen acitretine en nicotinamide
De hier beschreven onderzoeken laten verschillen zien in de gebruikte doseringen voor beide medicamenten. Dat maakt interpretatie van de resultaten lastig. Er worden wel nuttige aanbevelingen gedaan voor de dagelijkse praktijk: voor acitretine wordt geadviseerd te starten met 10 mg 1dd om de dag en deze dosering langzaam in 2 maanden tijd te verhogen naar de wenselijke onderhoudsdosering van 1dd 20 mg of 30 mg.6,14 Voor nicotinamide wordt 1 à 2dd 500 mg geadviseerd, waarbij 2dd doseren sneller tot effect leidt. Op de langere termijn lijken beide doseringen niet verschillend in effectiviteit.8 De effecten van beide therapieën zijn overigens aanwezig zo lang de middelen gebruikt worden. Bij staken gaan de positieve effecten weer verloren.2,3,14 Daarom lijkt chronische onderhoudsbehandeling noodzakelijk. Er zijn geen nadelen voor de nierfunctie of immuunsuppressielevels gevonden voor beide behandelingen in de verschillende studies.2-6, 9-11
Tot slot is een interessant weetje dat 5% topicale nicotinamide in een lotion beschermt tegen zowel UV-B als UV-A. Het wordt zelfs al als additief gebruikt in zonnebrandmiddelen, die op hun beurt uiteraard de basis van chemopreventie zullen blijven.15,16
Conclusie
Bij chronische hoogrisico-NMSC-patiënten met constante ontwikkeling van nieuwe huidmaligniteiten kan systemische chemopreventie met acitretine of nicotinamide een goede overweging zijn. Nicotinamide is een veilig, goedkoop en makkelijk verkrijgbaar middel, dat wellicht enige voorkeur geniet. Een review van Darmian is een goed artikel om de ‘ins and outs’ van nicotinamide in het kader van chemopreventie voor NMSC nog eens op een rijtje te zien.8
Bronnen:
- Rogers HW, Weinstock MA, Feldman SR, Coldiron BM. Incidence estimate of nonmelanoma skin cancer (keratinocyte carcinomas) in the US population. JAMA Dermatol 2015; 151(10): 1081-62.
- Chen AC, Martin AJ, Choy B, et al. A phase 3 randomized trial of nicotinamide for skin-cancer chemoprevention. N Engl J Med 2015; 373(17): 1618-26.
- Harwood CA, Leedham-Green M, Leigh IM, Proby CM. Low-dose retinoids in the prevention of cutaneous squamous cell carcinomas in organ transplant recipients: a 16-year retrospective study. Arch Dermatol 2005; 141(4): 456-64.
- Bavinck JN, Tieben LM, Van der Woude FJ, et al. Prevention of skin cancer and reduction of keratotic skin lesions during acitretin therapy in renal transplant recipients: a double-blind, placebo-controlled study. J Clin Oncol 1995; 13(8): 1933-8
- George R, Weightman W, Russ GR, et al. Acitretin for chemoprevention of non-melanoma skin cancers in renal transplant recipients. Australas J Dermatol 2002; 43(4): 269-73.
- Cornejo CM, Jambusaria-Pahlajani A, Willenbrink TJ, et al. Field cancerization: Treatment. J Am Acad Dermatol 2020; 83(3): 719-730.
- Fania L, Mazzanti C, Campione E, et al. Role of nicotinamide in genomic stability and skin cancer chemoprevention. Int J Mol Sci 2019; 20(23).
- Damian DL. Nicotinamide for skin cancer chemoprevention. Australas J Dermatol 2017; 58(3): 174-180.
- Drago F, Ciccarese G, Parodi A. Nicotinamide for skin-cancer chemoprevention. N Engl J Med 2016; 374: 789–90.
- Drago F, Ciccarese G, Cogorno L, et al. Prevention of non-melanoma skin cancers with nicotinamide in transplant recipients: a case-control study. Eur J Dermatol 2017; 27(4): 382-385.
- Chen AC, Martin AJ, Dalziell RA, et al. A phase 2 randomised controlled trial of nicotinamide for skin cancer chemoprevention in renal transplant recipients. Br J Dermatol 2016; 175: 1073–5.
- Tee LY, Sultana R, Tam SY, Oh CC. Chemoprevention of keratinocyte carcinoma and actinic keratosis in solid-organ transplant recipients: Systematic review and meta-analyses. J Am Acad Dermatol 2021; 84(2): 528-530.
- Hoegler KM, Khachemoune A. Is the first-line systemic chemoprevention of nonmelanoma skin cancer nicotinamide or acitretin? Int J Dermatol 2021; Feb 9. doi: 10.1111/ijd.15442.
- Otley CC, Stasko T, Tope WD, Lebwohl M. Chemoprevention of nonmelanoma skin cancer with systemic retinoids: practical dosing and management of adverse effects. Dermatol Surg 2006; 32(4): 562-8.
- Thanos SM, Halliday GM, Damian DL. Nicotinamide reduces photodynamic therapy-induced immunosuppression in humans. Br J Dermatol 2012; 167(3): 631-6.
- Sivapirabu G, Yiasemides E, Halliday GM, et al. Topical nicotinamide modulates cellular energy metabolism and provides broad-spectrum protection against ultraviolet radiation-induced immunosuppression in humans. Br J Dermatol 2009; 161(6): 1357-64.