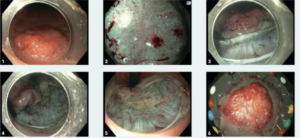
Een 65-jarige man werd verwezen in verband met de verdenking op een vroegcarcinoom van het rectum. Tijdens diagnostische scopie werd op 2 cm van de linea dentata een vlak verheven afwijking van circa 25 mm gezien met een centrale depressie (foto 1). Nadere inspectie van pit- en vaatpatroon met narrow band imaging (NBI) toonde duidelijke aanwijzingen voor diepere submucosale invasie met een amorf Kudo Vn pitpatroon en een sterk onregelmatig (Hiroshima C3) vaatpatroon (foto 2). Er werden geen biopten genomen. De MRI rectum liet een T1/2-tumor zien in het lage rectum zonder suspecte lymfeklieren locoregionaal.
Gezien de optische verdenking op diepere submucosale invasie werd een endoscopische submucosale dissectie (ESD) niet geschikt geacht vanwege hoge kans op een irradicale marge in het diepe resectievlak. Daarom werd een endoscopische intermusculaire dissectie (EID) voorgesteld.1 Deze nieuwe endoscopische resectietechniek is een afgeleide van de ESD, waarbij de dissectie niet in de submucosa (zoals bij ESD), maar in het vlak tussen de binnenste circulaire en buitenste longitudinale spierlaag (de intermusculaire ruimte) wordt verricht (foto 3 en 4). Door het meenemen van de binnenste circulaire spierlaag in het resectiepreparaat kan een radicale diepe resectiemarge worden bereikt voor tumoren die diep in de submucosa doorgroeien. Hierbij blijft de buitenste longitudinale spierlaag en daarmee de rectumwand intact (foto 5). Gezien de sterk ontwikkelde spierlaag van het rectum is deze techniek uitsluitend geschikt voor rectale laesies.
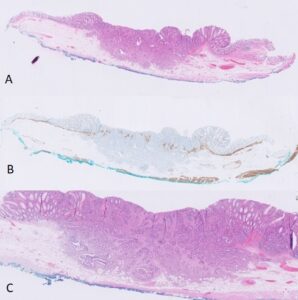
De procedure verliep technisch succesvol en zonder complicaties met een endoscopisch radicale resectie van de tumor (foto 6). De patiënt werd dezelfde dag naar huis ontslagen. Histopathologisch onderzoek toonde een goed tot matig gedifferentieerd adenocarcinoom dat reikte tot diep in de submucosa (sm3), waarbij alle snijvlakken vrij waren (foto 7). Er waren geen aanwijzingen voor lymfovasculaire invasie of hooggradige tumorbudding. De behandeling kan daarmee beschouwd worden als een curatieve resectie.
Inmiddels is de patiënt één jaar in follow-up, waarbij zowel MRI, CEA en endoscopie geen aanwijzingen voor recidief tonen (foto 8).
- Moons LMG, Bastiaansen BAJ, Richir MC, et al. Endoscopic intermuscular dissection for deep submucosal invasive cancer in the rectum: a new endoscopic approach. Endoscopy. 2022 Jan 24. doi: 10.1055/a-1748-8573. Online ahead of print.
Drs. Barbara Bastiaansen, MDL arts, Amsterdam UMC
Drs. Sander Albers, arts-onderzoeker, Amsterdam UMC
Dr. Leon M.G. Moons, MDL arts, UMC Utrecht
Commentaar Jacques Bergman
Diep submucosale rectumtumoren waren lange tijd een ‘no-go’ voor curatieve endoscopische behandeling. Daarnaast was endoscopische submucosale dissectie van diepe submucosale invasieve laesies technisch veelal onmogelijk door het ontbreken van een marge tussen tumor en spierlaag. De hier beschreven intermusculaire dissectie is een prachtige elegante extensie van de ESD-techniek. Hierdoor is een radicale endoscopische resectie ook voor diepe submucosale en vroege T2-tumoren haalbaar.
Inmiddels zijn in UMC Utrecht en Amsterdam UMC ruim 140 patiënten met deze techniek behandeld wat in 70% van de gevallen tot een rectumsparende behandeling heeft geleid. Een recente meta-analyse (Zwager et al, Gastroenterology 2022) laat zien dat diepte-invasie geen onafhankelijke risicofactor is voor lokale lymfekliermetastasering: de aard van de tumor (lymfangio-invasie, budding en differentiatie-graad) lijkt vele malen belangrijker dan diepte-invasie. Zonder dergelijke risicofactoren lijkt het risico op lokale lymfekliermetastasering < 3%. Een blijvertje dus deze intermusculaire dissectie!
- Fluorescentie-endoscopie voor snel en betrouwbaar diagnosticeren van voorstadia van slokdarmkanker
- Succesvolle ESD-procedure na stapsgewijze endoscopische dilatatie
- Dyspneu door achalasie
- Een naar de slokdarm gemigreerde siliconen Angelchik-prothese
- Endoscopisch creëren van een choledochoduodenostomie
- Robot-geassisteerde sentinel node-procedure na ESD voor hoog-risico early gastric cancer
- Endoscopic Ultrasound (EUS) geleide coiling voor een ernstige rectale varicesbloeding in combinatie met Histoacryl
- Intra-operatieve pancreatoscopie voor intraductaal papillair mucineus neoplasma (IPMN)
- Perorale endoscopische myotomie bij een patiënt met achalasie en een groot epifrenisch divertikel